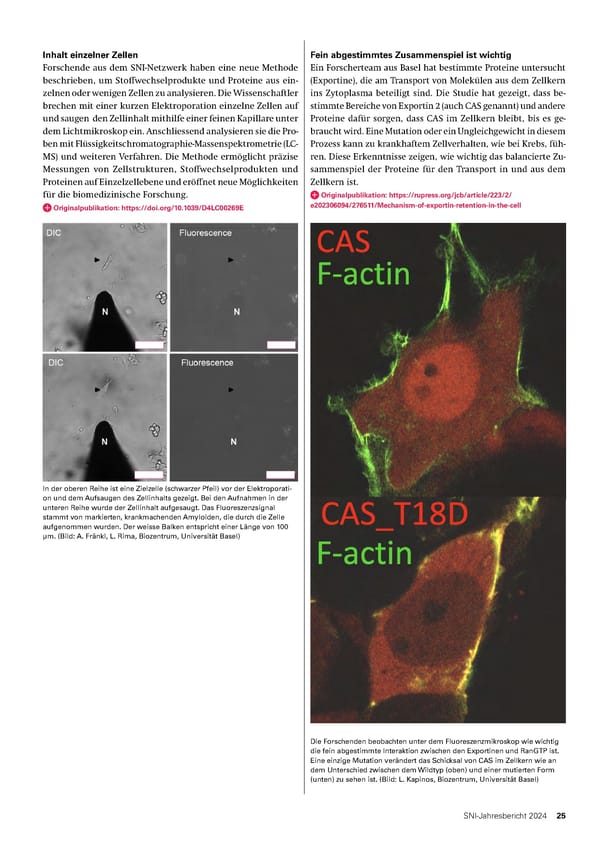
Inhalt einzelner Zellen Forschende aus dem SNI-Netzwerk haben eine neue Methode beschrieben, um Stoffwechselprodukte und Proteine aus ein- zelnen oder wenigen Zellen zu analysieren. Die Wissenschaftler brechen mit einer kurzen Elektroporation einzelne Zellen auf und saugen den Zellinhalt mithilfe einer feinen Kapillare unter dem Lichtmikroskop ein. Anschliessend analysieren sie die Pro- ben mit Flüssigkeitschromatographie-Massenspektrometrie (LC- MS) und weiteren Verfahren. Die Methode ermöglicht präzise Messungen von Zellstrukturen, Stoffwechselprodukten und Proteinen auf Einzelzellebene und eröffnet neue Möglichkeiten für die biomedizinische Forschung. Originalpublikation: https://doi.org/10.1039/D4LC00269E In der oberen Reihe ist eine Zielzelle (schwarzer Pfeil) vor der Elektroporati- on und dem Aufsaugen des Zellinhalts gezeigt. Bei den Aufnahmen in der unteren Reihe wurde der Zellinhalt aufgesaugt. Das Fluoreszenzsignal stammt von markierten, krankmachenden Amyloiden, die durch die Zelle aufgenommen wurden. Der weisse Balken entspricht einer Länge von 100 μm. (Bild: A. Fränkl, L. Rima, Biozentrum, Universität Basel) Fein abgestimmtes Zusammenspiel ist wichtig Ein Forscherteam aus Basel hat bestimmte Proteine untersucht (Exportine), die am Transport von Molekülen aus dem Zellkern ins Zytoplasma beteiligt sind. Die Studie hat gezeigt, dass be- stimmte Bereiche von Exportin 2 (auch CAS genannt) und andere Proteine dafür sorgen, dass CAS im Zellkern bleibt, bis es ge- braucht wird. Eine Mutation oder ein Ungleichgewicht in diesem Prozess kann zu krankhaftem Zellverhalten, wie bei Krebs, füh- ren. Diese Erkenntnisse zeigen, wie wichtig das balancierte Zu- sammenspiel der Proteine für den Transport in und aus dem Zellkern ist. Originalpublikation: https://rupress.org/jcb/article/223/2/ e202306094/276511/Mechanism of exportin retention in the cell Die Forschenden beobachten unter dem Fluoreszenzmikroskop wie wichtig die fein abgestimmte Interaktion zwischen den Exportinen und RanGTP ist. Eine einzige Mutation verändert das Schicksal von CAS im Zellkern wie an dem Unterschied zwischen dem Wildtyp (oben) und einer mutierten Form (unten) zu sehen ist. (Bild: L. Kapinos, Biozentrum, Universität Basel) 25 SNIJahresbericht 2024
 Jahresbericht 2024 - Swiss Nanoscience Institute Page 24 Page 26
Jahresbericht 2024 - Swiss Nanoscience Institute Page 24 Page 26